- COVID-19 එන්නතෙහි අතිරේක මාත්රාවක ආරක්ෂාව අධීක්ෂණය කිරීම පිළිබඳ CDC අධ්යයනය
- Th ගැන දැනටමත් දන්නා දේඊ බූස්ටර වෙඩි?
- ෆයිසර්-බයෝඑන්ටෙක් සායනික අත්හදා බැලීම් වලට සහභාගී වූ 306 දෙනා අතර, 3 මාත්රාවෙන් පසු අහිතකර ප්රතික්රියා 2 මාත්රාවට පසුව සමාන විය.
මෙම වාර්තාවෙන් එකතු කර ඇති දේ සීඩීසී විසින් නිකුත් කරන ලද අංක 3 දරණ වෙඩි තැබීම අද?
12 අගෝස්තු 19 සිට සැප්තැම්බර් 2021 දක්වා කාලය තුළ එම්ආර්එන්ඒ කෝවිඩ් -12,591 එන්නත මාත්රා 3 න් පසු සෞඛ්ය පරීක්ෂණ සමීක්ෂණයක් කළ v-ලියාපදිංචි ලියාපදිංචි කරුවන් 19 අතර පිළිවෙලින් 79.4% සහ 74.1% දේශීය හෝ පද්ධතිමය ප්රතික්රියා වාර්තා කළහ. තුන්වන මාත්රාව; 77.6% සහ 76.5% පිළිවෙලින් දෙවන මාත්රාවෙන් පසු දේශීය හෝ පද්ධතිමය ප්රතික්රියා වාර්තා කළහ.
පොදු සෞඛ්ය පුරුදු සඳහා වන බලපෑම් මොනවාද?
COVID-19 එන්නත අතිරේක මාත්රාවකින් පසු v- සේෆ් වෙත වූ ස්වේච්ඡා වාර්තාවල අනපේක්ෂිත ආකාරයේ අහිතකර ප්රතික්රියා දක්නට නොලැබුණි. අතිරේක COVID-19 මාත්රාවන් ඇතුළුව, සීඩීසී එන්නත වල ආරක්ෂාව නිරීක්ෂණය කරයි.
12 අගෝස්තු 2021 දින, ආහාර හා Administෂධ පරිපාලනය (එෆ්ඩීඒ) විසින් සුදුසුකම් ලත් පුද්ගලයින්ට ප්රාථමික එන්නත් මාලාවක් සම්පූර්ණ කිරීමෙන් පසු අතිරේක මාත්රාවක් පරිපාලනය කිරීම සඳහා ෆයිසර්-බයෝඑන්ටෙක් සහ මෝඩර්නා කොවිඩ් -19 එන්නත් සඳහා හදිසි අවස්ථා බලතල (ඊයූඒ) සංශෝධනය කළේය. මධ්යස්ථ සිට දැඩි ප්රතිශක්ති ප්රතිස්ථාපන කොන්දේසි (1,2) 22 සැප්තැම්බර් 2021 දින, දරුණු කොවිඩ් -6 සඳහා දැඩි අවදානමක් ඇති හෝ වෘත්තීයමය හෝ ආයතනික නිරාවරණය හේතුවෙන් වයස අවුරුදු 65 ට වැඩි පුද්ගලයින් අතර ප්රාථමික ශ්රේණිය අවසන් වී මාස 19 කට පසු ෆයිසර්-බයෝඑන්ටෙක් එන්නත අතිරේක මාත්රාවකට එෆ්ඩීඒ අවසර දුන්නේය. COVID-19 සඳහා ඉහළ අවදානමක් (1) ෆයිසර්-බයෝඑන්ටෙක් විසින් සිදු කරන ලද 3 වන අදියර සායනික පරීක්ෂණයේ ප්රතිඵල වලින් අවුරුදු 306-18 අතර පුද්ගලයින් 55 දෙනෙකු ඇතුළත් වූ අතර, මාත්රා 5 ක ප්රාථමික එම්ආර්එන්ඒ එන්නත් මාලාවක් අවසන් වී මාස 8-2 කට පසුව ලබා දුන් තුන්වන මාත්රාව ලැබීමෙන් පසු අහිතකර ප්රතික්රියා සමාන බව පෙන්නුම් කෙරිණි. මාත්රාව 2 ලැබීමෙන් පසු වාර්තා වූ අය; මෙම අහිතකර ප්රතික්රියා වලට මෘදු සිට මධ්යස්ථ එන්නත් කරන ස්ථානය සහ පද්ධතිමය ප්රතික්රියා ඇතුළත් වේ (3) සීඩීසී විසින් COVID-19 එන්නත ලබා දීමෙන් පසු ඇති විය හැකි අහිතකර ප්රතික්රියා පිළිබඳ තොරතුරු ලබා දීම සඳහා ස්වේච්ඡා, ස්මාර්ට් ජංගම දුරකථනය පදනම් කරගත් ආරක්ෂක නිරීක්ෂණ පද්ධතියක් වන v- ආරක්ෂිත ක්රමය සකස් කළේය.
ප්රතිශක්තිකරණය අඩු කොන්දේසි සහිත පුද්ගලයින් සඳහා අතිරේක මාත්රාවක් අනුමත කිරීමත් සමඟම, ලැබුණු COVID-19 එන්නතෙහි අතිරේක මාත්රාවන් පිළිබඳ තොරතුරු ලියාපදිංචිකරුවන්ට ඇතුළත් කර ගැනීම සඳහා v- ආරක්ෂිත වේදිකාව යාවත්කාලීන කරන ලදි. 12 අගෝස්තු 19 සිට සැප්තැම්බර් 2021 දක්වා කාලය තුළ, කොවිඩ් -22,191 එන්නත අතිරේක මාත්රාවක් ලැබුණු බව වාර්තා වී ඇති ආරක්ෂිත ආරක්ෂක ලියාපදිංචිකරුවන් සංඛ්යාව 19 කි. බොහෝ දෙනෙක් (97.6%) ප්රාථමික මාත්රා 2 ක එම්ආර්එන්ඒ එන්නත් මාලාවක් වාර්තා කළ අතර එම එන්නතේම තුන්වන මාත්රාව ද වාර්තා කළහ. මාත්රා 3 ම සඳහා (12,591; 58.1%) සෞඛ්ය පරීක්ෂණ සමීක්ෂණය සම්පූර්ණ කළ අය අතර, 79.4% සහ 74.1% පිළිවෙලින් දේශීය හෝ පද්ධතිමය ප්රතික්රියා වාර්තා කළ අතර, මාත්රාව 3 ට පසුව, දේශීය හෝ පද්ධතිමය වාර්තා කළ 77.6% හා 76.5% ට සාපේක්ෂව ප්රතික්රියා පිළිවෙලින් මාත්රාවෙන් පසු 2. මෙම මූලික සොයාගැනීම් මඟින් COVID-19 එන්නත අතිරේක මාත්රාවකට පසු බලාපොරොත්තු නොවූ ආකාරයේ අහිතකර ප්රතික්රියා ඇති නොවන බව පෙන්නුම් කරයි; මෙම අහිතකර ප්රතික්රියා වලින් වැඩි ප්රමාණයක් මෘදු හෝ මධ්යස්ථ විය. සීඩීසී අඛණ්ඩව කොවිඩ් -19 එන්නතෙහි අතිරේක මාත්රාවල ආරක්ෂාව ඇතුළුව එන්නත් වල ආරක්ෂාව අධීක්ෂණය කරන අතර එන්නත් නිර්දේශයන් මඟ පෙන්වීම සහ මහජන සෞඛ්ය ආරක්ෂා කිරීම සඳහා දත්ත ලබා දේ.
වී-සේෆ් යනු ස්වේච්ඡා ස්මාර්ට් ජංගම දුරකථනය පදනම් කරගත් එක්සත් ජනපද ආරක්ෂක නිරීක්ෂණ පද්ධතියකි; බලයලත් හෝ බලපත්රලත් එන්නත් නිෂ්පාදන ලබා ගැනීමට සුදුසුකම් ලත් එන්නත් කරුවන්ට v- ආරක්ෂිතව ලියාපදිංචි විය හැකිය. වී-ආරක්ෂිත වේදිකාව මඟින් දැනට සිටින ලියාපදිංචිකරුවන්ට අතිරේක කොවිඩ් -19 එන්නත මාත්රාවක් ලැබීම ගැන වාර්තා කිරීමට සහ ලැබුණු කොවිඩ් -19 එන්නත සියලුම මාත්රාවන් පිළිබඳව නව ලියාපදිංචිකරුවන්ට තොරතුරු ඇතුළත් කිරීමට ඉඩ සලසයි. සෑම එන්නතක්ම ලබා දීමෙන් පසු 0-7 දින තුළ වී-ආරක්ෂිත සෞඛ්ය සමීක්ෂණ යවන අතර දේශීය එන්නත් කරන ස්ථානය සහ පද්ධතිමය ප්රතික්රියා සහ සෞඛ්ය බලපෑම් පිළිබඳ ප්රශ්න ඇතුළත් වේ.* ඇතුළත් කළ නවතම මාත්රාව සඳහා සමීක්ෂණ යවනු ලැබේ.† එන්නත ලබා දීමෙන් පසු වෛද්ය ප්රතිකාර ලබා ගත් බව සඳහන් VAERS වාර්තා වාර්තාව සම්පූර්ණ කිරීමට දිරි දීම හෝ පහසුකම් සැලසීම පෙන්නුම් කරන එන්නත් අහිතකර සිදුවීම් වාර්තාකරණ පද්ධතියේ (VAERS) මාණ්ඩලික සාමාජිකයින්.§
19 අගෝස්තු 12 සිට සැප්තැම්බර් 19 දක්වා අතිරේක COVID-2021 එන්නත් මාත්රාවක් ලැබුණු බව වාර්තා කළ v-ආරක්ෂිත ලියාපදිංචිකරුවන් අතර, ජනගහන දත්ත, දේශීය හා පද්ධතිමය ප්රතික්රියා සහ 0-7 දින තුළ වාර්තා වූ සෞඛ්ය බලපෑම් එන්නත් කිරීමේ ක්රමය මඟින් විස්තර කෙරේ (එනම්. , එක් එක් මාත්රාව සඳහා එන්නත් නිෂ්පාදකයා). එක්සත් ජනපදයේ නොදන්නා හෝ ලබා ගත නොහැකි විවිධ නිෂ්පාදකයින්ගෙන් හෝ නිෂ්පාදකයින්ගෙන් ප්රාථමික ශ්රේණියක් ලබා ගත් බවට වාර්තා වූ පුද්ගලයින් හෝ ජැන්සන් (ජොන්සන් සහ ජොන්සන්) තනි මාත්රා එන්නතක් (2) ලැබීමෙන් පසු එන්නත් මාත්රා 150 ක් විශ්ලේෂණයෙන් බැහැර කර ඇත. අතිරේක මාත්රාව ලැබීමෙන් පසු අහිතකර ප්රතික්රියා.
ප්රාථමික එන්නත් මාලාව අවසන් වී අතිරේක මාත්රාවක් ලබා ගැනීමට ගත වූ කාලය එන්නත් කිරීමේ ක්රමය මඟින් විස්තර කෙරිණි. එකම නිෂ්පාදකයාගෙන් එම්ආර්එන්ඒ එන්නත ලබා ගත් ලියාපදිංචිකරුවන් සඳහා 2 සහ 3 මාත්රාවලින් පසුව ඇති අහිතකර සිදුවීම් පැතිකඩයන් එකම මාත්රාව 3 සඳහාම සංසන්දනය කරන ලදී.¶ සියලුම විශ්ලේෂණ සිදු කිරීම සඳහා එස්ඒඑස් මෘදුකාංගය (අනුවාදය 9.4; එස්ඒඑස් ආයතනය) භාවිතා කරන ලදී. මෙම නිරීක්ෂණ කටයුතු සීඩීසී විසින් සමාලෝචනය කරන ලද අතර අදාළ ෆෙඩරල් නීතිය සහ සීඩීසී ප්රතිපත්තියට අනුකූලව සිදු කරන ලදී. **
ප්රාථමික ශ්රේණිය අවසන් කිරීමෙන් පසු 12 අගෝස්තු 19 සිට සැප්තැම්බර් 2021 දක්වා කාලය තුළ v-ආරක්ෂිත ලියාපදිංචිකරුවන් 22,191 ක් අතිරේක COVID-19 එන්නත මාත්රාවක් ලැබුණු බව වාර්තා කළහ (වගුව 1) මේ අය අතර 14,048 (63.3%) ක් කාන්තාවන් වූ අතර දළ වශයෙන් 30% බැගින් වයස අවුරුදු 18-49, 50-64 සහ 65-74 අතර වයසේ පසුවෙති.
බොහෝ ලියාපදිංචිකරුවන් (21,662; 97.6%) වාර්තා කළේ මොඩර්නා ලබන්නන්ගෙන් 98.6% ක් සහ ෆයිසර්-බයෝඑන්ටෙක් ලබන්නන්ගෙන් 98.2% ක් ද ඇතුළුව, ඔවුන්ගේ මූලික එම්ආර්එන්ඒ එන්නත් මාලාවේ එකම නිෂ්පාදකයාගෙන් තුන්වන මාත්රාවක් ලැබුණු බවයි. ලියාපදිංචිකරුවන් ස්වල්ප දෙනෙක් (341; 1.5%) ප්රාථමික එම්ආර්එන්ඒ එන්නත් මාලාවක් වාර්තා කළ අතර පසුව වෙනත් නිෂ්පාදකයෙකුගෙන් එම්ආර්එන්ඒ එන්නත අතිරේක මාත්රාවක්, ප්රාථමික එම්ආර්එන්ඒ එන්නත් මාලාවක් ලැබීමෙන් පසු ජැන්සන් එන්නත මාත්රාවක් (10; 0.05%) හෝ අතිරේකව ජෑන්සන් එන්නතෙන් පසු ඕනෑම නිෂ්පාදකයෙකුගෙන් COVID-19 එන්නත මාත්රාව (178; 0.8%).
22,191 v- ආරක්ෂිත ලියාපදිංචිකරුවන් අතර, ප්රාථමික COVID-19 එන්නත් මාලාව සම්පූර්ණ කිරීමේ සිට අතිරේක මාත්රාවක් ලබා ගැනීමේ මධ්ය පරතරය දින 182 කි (අන්තර් චතුරශ්ර පරාසය [IQR] = දින 160-202) (වගුව 2) ජැන්සන් එන්නත මාත්රා 2 ක් ලබා ගත් අය අතර, මාත්රාවන් අතර මධ්ය පරතරය කෙටි විය (දින 84; IQR = දින 16-136).
අතිරේක (COVID-16,615) එන්නත ලබා ගත් සතියේදී දේශීය (74.9; 15,503%) සහ පද්ධතිමය (69.9; 19%) ප්රතික්රියා නිතර නිතර වාර්තා විය, බොහෝ විට එන්නත ලබා දුන් දිනට පසු දින. නිතර වාර්තා වන ප්රතික්රියා නම් එන්නත් කරන ස්ථානයේ වේදනාව (15,761; 71.0%), තෙහෙට්ටුව (12,429; 56.0%) සහ හිසරදය (9,636; 43.4%) ය.
අතිරේක මාත්රා ලබන්නන් 22,191 ක් අතර, 7,067 ක් (31.8%) සෞඛ්ය බලපෑම් වාර්තා කර ඇති අතර, ආසන්න වශයෙන් 28.3% ක් (6,287) වාර්තා කළේ, සාමාන්යයෙන් එන්නත ලබා දුන් දිනට පසු දින ඔවුන්ට සාමාන්ය දෛනික කටයුතු කිරීමට නොහැකි වූ බවයි. ලියාපදිංචිකරුවන් 401 (1.8%) ක් වෛද්ය ප්රතිකාර ලබා ගත් අතර දහතුන් දෙනෙකු (0.1%) රෝහල් ගත කර ඇත. V- ආරක්ෂිත සමීක්ෂණයෙන් වෛද්ය ප්රතිකාර ලබා ගැනීමට හෝ රෝහල් ගත වීමට හේතු හඳුනාගෙන නොමැත; කෙසේ වෙතත්, එන්නත ලබා දීමෙන් පසු වෛද්ය ප්රතිකාර ලබා ගත් බව සඳහන් ලියාපදිංචිකරුවන්ට VAERS කාර්ය මණ්ඩලය සම්බන්ධ වී VAERS වාර්තාවක් සම්පුර්ණ කරන ලෙස දිරිමත් කෙරේ.
මාත්රා 21,658 ම සඳහා එකම එම්ආර්එන්ඒ එන්නත ලබා ගත් v- ආරක්ෂිත ලියාපදිංචිකරුවන් 3 දෙනා අතර 12,591 ක් (58.1%) 0-7 වැනි දින තුළ අවම වශයෙන් එක් සෞඛ්ය පරීක්ෂණ සමීක්ෂණයක් හෝ මාත්රා 3 න් පසු අවසන් කළහ; මාත්රාව 79.4 ට පසු පිළිවෙලින් 74.1% සහ 3% දේශීය හෝ පද්ධතිමය ප්රතික්රියා වාර්තා කළ අතර, මාත්රාවෙන් පසු පිළිවෙලින් දේශීය හා පද්ධතිමය ප්රතික්රියා වාර්තා කළ 77.6% සහ 76.5% ට සාපේක්ෂව 2. මොඩර්නා මාත්රා 3 ක් ලබා ගත් ලියාපදිංචිකරුවන් අතර (6,283), දේශීය මාත්රාව 3 ට වඩා මාත්රාව 2 න් පසු ප්රතික්රියා නිතර නිතර වාර්තා විය (5,323; 84.7% සහ 5,249; 83.5%; p- අගය = 0.03) (රූපය) මාත්රාව 3 ට පසුව 2 මාත්රාවට වඩා අඩු වාර ගණනක් පද්ධතිමය ප්රතික්රියා වාර්තා විය (4,963; 79.0% සහ 5,105; 81.3%; p- අගය <0.001).
ෆයිසර්-බයෝඑන්ටෙක් (3) මාත්රා 6,308 ක් ලබා ගත් ලියාපදිංචිකරුවන් අතර, මාත්රාව 3 ට වඩා 2 (4,674; 74.1% සහ 4,523; 71.7%; p- අගය <0.001) ට වඩා වැඩි වාර ගණනක් දේශීය ප්රතික්රියා වාර්තා විය. මාත්රාව 3 න් 2 ට අඩු (4,363; 69.2% සහ 4,524; 71.7%; p- අගය <0.001) ට වඩා අඩු වාර ගණනක් ක්රමානුකූල ප්රතික්රියා වාර්තා විය. එම්ආර්එන්ඒ එන්නතෙහි මාත්රාව 3 න් පසු වේදනාව වාර්තා කළ අය අතර බොහෝ ප්රතික්රියා මෘදු (4,909; 51.4%) හෝ මධ්යස්ථ (4,000; 41.9%) විය; දැඩි වේදනාව (දෛනික කටයුතු දුෂ්කර හෝ කළ නොහැකි වේදනාවක් ලෙස අර්ථ දැක්වේ) 637 (6.7%) විසින් වාර්තා කරන ලදී.
සාකච්ඡා
19 සැප්තැම්බර් 2021 වන විට එක්සත් ජනපදයේ දළ වශයෙන් මිලියන 2.21 ක පුද්ගලයින්ට COVID-19 එන්නත් අතිරේක මාත්රාවන් ලැබී තිබුණි.†† ප්රාථමික මාලාවක් අවසන් කිරීමෙන් පසුව. 12 අගෝස්තු 19 සිට සැප්තැම්බර් 2021 දක්වා, කොවිඩ් -22,191 එන්නත අතිරේක මාත්රාවක් ලබා ගත් වි-ආරක්ෂිත ලියාපදිංචි වූ 19 අතර අනපේක්ෂිත ආකාරයේ අහිතකර ප්රතික්රියා දක්නට නොලැබුණි. බොහෝ විට වාර්තා වූ දේශීය හා පද්ධතිමය ප්රතික්රියා මෘදු සිට මධ්යස්ථ, තාවකාලික වන අතර එන්නත ලබා දුන් දිනට පසු දින බොහෝ විට වාර්තා වේ. අතිරේක මාත්රාවක් ලබා ගත් බොහෝ ලියාපදිංචිකරුවන් විසින් මූලික එම්ආර්එන්ඒ එන්නත් මාලාවක් වාර්තා කළ අතර තුන්වන මාත්රාව එකම නිෂ්පාදකයාගෙන් වාර්තා විය.
වයස අවුරුදු 306-18 අතර පුද්ගලයින් 55 ක් ඇතුළත් ෆයිසර්-බයෝඑන්ටෙක් සායනික පරීක්ෂණයෙන් පෙන්නුම් කළේ මාත්රාව 3 න් පසු ප්රතික්රියා 2 මාත්රාවෙන් පසු වාර්තා වූ ඒවාට සමාන කළ හැකි බවයි (3) කෙසේ වෙතත්, වී-ආරක්ෂිත දත්ත විශ්ලේෂණය කිරීමේදී ෆයිසර්-බයෝඑන්ටෙක් හි මාත්රාව 3 න් පසු දේශීය ප්රතික්රියා තරමක් පොදු වන අතර පද්ධතිමය ප්රතික්රියා අඩු බව සොයා ගන්නා ලදී.
මොඩර්නා එන්නත හෝ ෆයිසර්-බයෝඑන්ටෙක් මාත්රාව 3 න් පසුව නිරීක්ෂණය කරන ලද අහිතකර ප්රතික්රියා වල රටාවන් මාත්රාව 2 ලැබීමෙන් පසු කලින් විස්තර කළ ප්රතික්රියා වලට අනුකූල වේ.
ජැන්සන් එන්නත මාත්රාවන් 2 ක් ලබා ගත් බව හෝ ඔවුන්ගේ මූලික ශ්රේණියට වඩා වෙනස් නිෂ්පාදකයෙකුගෙන් ඔවුන්ගේ අතිරේක මාත්රාව ලබා ගත් බව සඳහන් කළ ලියාපදිංචි අයගේ සංඛ්යාව කුඩා වූ අතර ඕනෑම නිගමනයකට සීමා වේ.
විවිධ නිෂ්පාදකයින්ගේ කොවිඩ් -19 එන්නත් නිෂ්පාදන සමඟ එන්නත් කිරීමේ ආරක්ෂාව හෝ ඵලදායීතාවය පිළිබඳ දත්ත සීමිත ය; ප්රතිශක්තිකරණ පුරුදු පිළිබඳ උපදේශක කමිටුව (ඒසීඅයිපී) නිර්දේශ කරන්නේ මධ්යස්ථව සිට දැඩි ලෙස ප්රතිශක්තිකරණයට යටත් නොවන තත්වයන් ඇති පුද්ගලයින්ට ඔවුන්ගේ මූලික ශ්රේණියේම එම නිෂ්පාදකයාගෙන්ම එම්ආර්එන්ඒ කෝවිඩ් -19 එන්නතෙහි තුන්වන මාත්රාව ලබා ගත යුතු බවයි.
අතිරේක මාත්රාවක් සඳහා සීඩීසී නිර්දේශ වලට දැනට ජැන්සන් එන්නත ලබා ගත් පුද්ගලයින් ඇතුළත් නොවේ.
මෙම අධ්යයනයෙන් ආවරණය වූ කාල සීමාව තුළ, අතිරේක COVID-19 එන්නත මාත්රාවක් සඳහා වූ ACIP නිර්දේශ මධ්යස්ථ හා දැඩි ලෙස ප්රතිශක්තිකරණයට ලක් වූ කොන්දේසි සහිත පුද්ගලයින්ට සීමා විය.
එම්ආර්එන්ඒ එන්නත මාත්රා 2 ක්.
ප්රතිශක්තිකරණයට ලක් නොවූ රක්තපාත රෝගීන් අතර සිදු කරන ලද අධ්යයනයකින් හෙළි වූයේ ෆයිසර්-බයෝඑන්ටෙක් එන්නතෙහි 3 මාත්රාවෙන් පසු දේශීය හා පද්ධතිමය ප්රතික්රියා 2 මාත්රාවට පසුව සමාන බවයි.. එන්නත් කරන ලද පුද්ගලයින්ගේ ආසාදන පිළිබඳ මෑත කාලීන වාර්තා සහ SARS-CoV-1.617.2 හි B.2 (Delta) ප්රභේදය සමඟ ආසාදනය පැතිරීම, එන්නත් කළ පුද්ගලයින් අතර COVID-19 ඇති කරන වෛරසය, සමහර පුද්ගලයින් සෙවීමට පොළඹවා ඇත. නිර්දේශයෙන් පිටත අතිරේක මාත්රාවක්. ප්රාථමික ශ්රේණිය සම්පූර්ණ කිරීමේ සිට අතිරේක මාත්රාවක් ලැබීම දක්වා වූ මධ්ය විරාමය ආසන්න වශයෙන් මාස 6ක් විය; එබැවින්, සෞඛ්ය සේවකයින් සහ වැඩිහිටි වැඩිහිටියන් ඇතුළු COVID-19 එන්නත් නිකුත් කිරීමේදී ප්රමුඛත්වය දුන් පුද්ගලයින්ට අමතර මාත්රාවක් ලැබිය හැකිය.
මෙම වාර්තාවේ සොයා ගැනීම් අවම වශයෙන් සීමා හතරකට යටත් වේ. පළමුවෙන්ම, v- සේප්පුවට ඇතුළත් වීම ස්වේච්ඡාවෙන් සිදු වන අතර එන්නත ලබා ගත් එක්සත් ජනපද ජනගහනයේ නියෝජිතයෙකු නොවේ; සහභාගී වූවන්ගෙන් වැඩි දෙනෙක් තමන් සුදු ජාතිකයින් සහ හිස්පැනික් නොවන අය ලෙස හඳුනා ගත්හ. දෙවනුව, මෙම අධ්යන කාලය තුළදී, අතිරේක මාත්රා නිර්දේශ ප්රාථමික එම්ආර්එන්ඒ කෝවිඩ් -19 එන්නත් කිරීමේ මාලාවක් සම්පූර්ණ කළ ප්රතිශක්තිකරණය අඩු කොන්දේසි සහිත පුද්ගලයින්ට සීමා විය; කෙසේ වෙතත්, v- ආරක්ෂක ප්රතිශක්තිකරණ තත්ත්වය පිළිබඳ තොරතුරු ඇතුළත් නොවේ.
අතිරේක මාත්රා ලබන්නන් තුළ ප්රතිශක්ති සම්මුති විරහිත තත්ත්වයන් ඇති සහ නැති පුද්ගලයින් ඇතුළත් විය හැකිය. තෙවනුව, එන්නත ලබා දීමෙන් පසු වාර්තා වූ එන්නත සහ සායනික වශයෙන් අහිතකර අහිතකර සිදුවීම් අතර හේතු-සම්බන්ධතාව v- ආරක්ෂිත දත්ත භාවිතයෙන් තහවුරු කර ගත නොහැක. අවසාන වශයෙන්, ප්රාථමික ශ්රේණියට හෝ ජැන්සන් එන්නතට වෙනස් නිෂ්පාදකයෙකුගෙන් අතිරේක මාත්රාවක් ලැබීමෙන් පසු අහිතකර ප්රතික්රියා වල රටාවන් නිශ්චය කර ගැනීමට ප්රමාණවත් දත්ත නොමැත.
මධ්යස්ථ හා දැඩි ලෙස ප්රතිශක්ති ප්රතිශක්තිකරණයට ගොදුරු වන තත්වයන් ඇති පුද්ගලයින් සඳහා එම්ආර්එන්ඒ කෝවිඩ් -19 එන්නත අතිරේක මාත්රාවක් නිර්දේශ කෙරේ (5).
වයස අවුරුදු 6 ට වැඩි පුද්ගලයින්, දිගු කාලීන සත්කාර මධ්යස්ථාන වල පදිංචිකරුවන් සහ අවුරුදු 65-50 අතර වයස්ගත වූ රෝගී තත්වයන් ඇති පුද්ගලයින් අතර ප්රාථමික එන්නත් මාලාව අවසන් වී මාස 64 කට පසු ෆයිසර්-බයෝඑන්ටෙක් එන්නත අතිරේක මාත්රාවක් සීඩීසී නිර්දේශ කළේය; වෘත්තීයමය හෝ ආයතනික සැකසීම හේතුවෙන් වයස අවුරුදු 18-49 අතර වයස්ගත පුද්ගලයින්ට සහ වෘත්තීයමය හෝ ආයතනික සැකසුම් හේතුවෙන් COVID-18 නිරාවරණය වීමේ සහ සම්ප්රේෂණය වීමේ වැඩි අවදානමක් ඇති අවුරුදු 64-19 අතර පුද්ගලයින්ට ඔවුන්ගේ පුද්ගලික ප්රතිලාභ සහ අවදානම් මත පදනම්ව අතිරේක මාත්රාවක් ලැබිය හැකිය.
ආරක්ෂිත ලියාපදිංචිකරුවන්ගේ> 22,000 සිට ආරක්ෂිත දත්ත පිළිබඳ මූලික විශ්ලේෂණයන් මඟින් පෙන්නුම් කරන්නේ එම්ආර්එන්ඒ මාත්රාව 3 ට පසුව දේශීය ප්රතික්රියාවන් සුළු වශයෙන් වැඩි වී ඇති බවත් පද්ධතිමය ප්රතික්රියා සුළු වශයෙන් අඩු වන බවත්ය.
අහිතකර ප්රතික්රියා වල අනපේක්ෂිත රටා හඳුනා නොගත්තේය; වාර්තා වූ ඒවා මෘදු සිට මධ්යස්ථ හා සංක්රාන්ති විය. සීඩීසී විසින් කොවිඩ් -19 එන්නතෙහි අතිරේක මාත්රාවල ආරක්ෂාව අඛණ්ඩව අධීක්ෂණය කරනු ඇත. පොදු සෞඛ්ය නිර්දේශයන් මඟ පෙන්වීම සඳහා මූලික එන්නත් වල විවිධ සංයෝජන හා ප්රාථමික ශ්රේණි අවසන් වීමෙන් පසු ඇති වන අහිතකර ප්රතික්රියා පිළිබඳ අතිරේක දත්ත වැදගත් වනු ඇත.
| ලාක්ෂණික | මෝඩර්නා, %† (n = 10,601) | ෆයිසර්-බයෝඑන්ටෙක්, %† (n = 11,412) | ජැන්සන්, %, § (n = 178) | මුළු (N = 22,191) | ||||||
|---|---|---|---|---|---|---|---|---|---|---|
| මාත්රාව 3 මාදිලිය (n = 10,453; 98.6%) | මාත්රාව 3 ෆයිසර්-බයෝඑන්ටෙක් (n = 144; 1.4%) | මාත්රාව 3 ජෑන්සන් (n = 4; 0.04%) | මාත්රාව 3 ෆයිසර්-බයෝඑන්ටෙක් (n = 11,209; 98.2%) | මාත්රාව 3 මාදිලිය (n = 197; 1.7%) | මාත්රාව 3 ජෑන්සන් (n = 6; 0.1%) | මාත්රාව 2 ජෑන්සන් (n = 48; 27.0%) | මාත්රාව 2 මාදිලිය (n = 64; 36.0%) | මාත්රාව 2 ෆයිසර්-බයෝඑන්ටෙක් (n = 66; 37.1%) | ||
| ලිංගික කාරණා | ||||||||||
| කාන්තා | 63.8 | 63.9 | 50.0 | 63.0 | 63.5 | 33.3 | 39.6 | 57.8 | 59.1 | 63.3 |
| පිරිමි | 35.1 | 34.0 | 50.0 | 36.1 | 36.0 | 66.7 | 60.4 | 42.2 | 40.9 | 35.7 |
| නොදන්නා | 1.0 | 2.1 | 0 | 0.9 | 0.5 | 0 | 0 | 0 | 0 | 1.0 |
| වයස් කණ්ඩායම, අවුරුදු | ||||||||||
| 0-17 | 0.0 | 0.7 | 0.0 | 0.6 | 0.0 | 0.0 | 0.0 | 0.0 | 0.0 | 0.3 |
| 18-49 | 25.7 | 36.1 | 25.0 | 31.5 | 42.6 | 50.0 | 54.2 | 60.9 | 57.6 | 29.1 |
| 50-64 | 28.4 | 27.1 | 50.0 | 31.1 | 29.9 | 0.0 | 33.3 | 34.3 | 30.3 | 29.8 |
| 65-74 | 33.9 | 27.1 | 0.0 | 27.8 | 21.3 | 50.0 | 10.4 | 4.7 | 9.1 | 30.5 |
| 75-84 | 10.9 | 9.0 | 25.0 | 8.3 | 5.6 | 0.0 | 2.1 | 0.0 | 3.0 | 9.5 |
| ≥85 | 1.1 | 0.0 | 0.0 | 0.7 | 0.5 | 0.0 | 0.0 | 0.0 | 0.0 | 0.9 |
| ජනවාර්ගිකත්වය | ||||||||||
| ස්පාඤ්ඤ / ලතින් | 8.0 | 15.3 | 0 | 8.2 | 5.6 | 0 | 25.0 | 6.3 | 10.6 | 8.2 |
| හිස්පැනික් නොවන/ලතින් | 87.7 | 81.9 | 100 | 87.6 | 90.9 | 100 | 54.2 | 89.1 | 89.4 | 87.6 |
| නොදන්නා | 4.3 | 2.8 | 0 | 4.2 | 3.6 | 0 | 20.8 | 4.7 | 0 | 4.2 |
| තරඟය | ||||||||||
| AI/AN | 0.5 | 0.7 | 0 | 0.5 | 0.5 | 0 | 2.1 | 0 | 0 | 0.5 |
| ආසියානු | 4.9 | 5.6 | 0 | 6.1 | 7.1 | 0 | 2.1 | 14.1 | 13.6 | 5.6 |
| කලු | 5.6 | 3.5 | 0 | 6.2 | 1.5 | 16.7 | 6.3 | 6.3 | 9.1 | 5.9 |
| එන්එච්පීඅයි | 0.2 | 0 | 0 | 0.3 | 0.5 | 0 | 4.2 | 0 | 0 | 0.3 |
| සුදු | 82.6 | 82.6 | 100 | 80.4 | 85.8 | 66.7 | 56.3 | 71.9 | 69.7 | 81.4 |
| බහු වාර්ගික | 1.9 | 2.1 | 0 | 1.8 | 1.5 | 16.7 | 4.2 | 4.7 | 3.0 | 1.9 |
| වෙනත් | 2.1 | 4.2 | 0 | 2.1 | 0.5 | 0 | 6.3 | 1.6 | 3.0 | 2.1 |
| නොදන්නා | 2.3 | 1.4 | 0 | 2.5 | 2.5 | 0 | 18.8 | 1.6 | 1.5 | 2.4 |
සංක්ෂිප්ත: AI/AN = ඇමරිකානු ඉන්දියානු/ඇලස්කාවේ ස්වදේශිකයා; NHPI = ස්වදේශික හවායි හෝ වෙනත් පැසිෆික් දූපත් වැසියන්.
* එන්නත ලබා දීමෙන් පසු 0-7 දින තුළ අවම වශයෙන් v- ආරක්ෂිත සෞඛ්ය පරීක්ෂණ සමීක්ෂණයක් සම්පූර්ණ කළ ලියාපදිංචිකරුවන්ගේ ප්රතිශතය.
† මූලික එන්නත් මාලාව.
§ ලැයිස්තුගත නිෂ්පාදකයින්ගෙන් ප්රාථමික ජැන්සන් තනි මාත්රාවක් සහ අතිරේක එන්නත් මාත්රාවක් ලබා ගත් පුද්ගලයින් ඇතුළත් වේ.
| ප්රතික්රියාව | මෝඩර්නා, %† (n = 10,477) | ෆයිසර්-බයෝඑන්ටෙක්, %† (n = 11,284) | ජැන්සන්, %, § (n = 174) | මුළු (N = 22,191) | ||||||
|---|---|---|---|---|---|---|---|---|---|---|
| මාත්රාව 3 මාදිලිය (n = 10,453; 98.6%) | මාත්රාව 3 ෆයිසර්-බයෝඑන්ටෙක් (n = 144; 1.4%) | මාත්රාව 3 ජෑන්සන් (n = 4; 0.04%) | මාත්රාව 3 ෆයිසර්-බයෝඑන්ටෙක් (n = 11,209; 98.2%) | මාත්රාව 3 මාදිලිය (n = 197; 1.7%) | මාත්රාව 3 ජෑන්සන් (n = 6; 0.1%) | මාත්රාව 2 ජෑන්සන් (n = 48; 27.0%) | මාත්රාව 2 මාදිලිය (n = 64; 36.0%) | මාත්රාව 2 ෆයිසර්-බයෝඑන්ටෙක් (n = 66; 37.1%) | ||
| ප්රාථමික ශ්රේණියේ සිට මධ්ය, (IQR) | 182 (164 - 198) | 183 (161 - 204) | 173 (141 - 182) | 183 (157 - 209) | 186 (161 - 217) | 123 (113 - 182) | 84 (16 - 136) | 156 (140 - 164) | 150 (136 - 167) | 182 (160 - 202) |
| එන්නත් කරන ස්ථානයේ ඕනෑම ප්රතික්රියාවක් | 80.9 | 64.6 | 75.0 | 69.4 | 81.7 | 83.3 | 25.0 | 70.3 | 80.3 | 74.9 |
| කැසීම | 20.0 | 11.8 | 0 | 8.4 | 10.2 | 16.7 | 10.4 | 6.3 | 7.6 | 13.9 |
| වේදනාව | 75.9 | 60.4 | 75.0 | 66.6 | 80.2 | 83.3 | 20.8 | 68.8 | 74.2 | 71.0 |
| රතු පැහැය | 25.2 | 8.3 | 0 | 9.8 | 20.8 | 16.7 | 6.3 | 7.8 | 12.1 | 17.1 |
| ඉදිමීම | 33.6 | 17.4 | 0 | 16.8 | 30.5 | 16.7 | 6.3 | 12.5 | 18.2 | 24.8 |
| ඕනෑම පද්ධතිමය ප්රතික්රියාවක් | 75.2 | 59.7 | 50.0 | 65.1 | 76.1 | 100 | 31.3 | 68.8 | 63.6 | 69.9 |
| බඩේ වේදනාව | 8.4 | 3.5 | 0 | 6.4 | 8.1 | 16.7 | 4.2 | 3.1 | 6.1 | 7.3 |
| මයිල්ජියා | 49.8 | 29.2 | 0 | 36.3 | 49.2 | 50.0 | 20.8 | 45.3 | 33.3 | 42.7 |
| මෝඩයෝ | 31.3 | 8.3 | 50.0 | 17.5 | 33.5 | 50.0 | 8.3 | 23.4 | 10.6 | 24.1 |
| පාචනය | 9.9 | 7.6 | 0 | 9.0 | 9.6 | 16.7 | 8.3 | 6.3 | 9.1 | 9.4 |
| ආකෘතිය | 61.8 | 44.4 | 0 | 51.0 | 60.9 | 83.3 | 14.6 | 48.4 | 50.0 | 56.0 |
| උණ | 36.4 | 20.1 | 50.0 | 22.2 | 37.1 | 50.0 | 6.3 | 37.5 | 12.1 | 29.0 |
| හිසරදය | 49.0 | 31.1 | 0 | 38.4 | 49.7 | 83.3 | 18.8 | 35.9 | 40.9 | 43.4 |
| හන්දිපත් රුදාව | 33.0 | 18.8 | 0 | 23.0 | 31.0 | 33.3 | 16.7 | 20.3 | 19.7 | 27.7 |
| ඔක්කාරය | 18.8 | 10.4 | 25.0 | 13.6 | 21.3 | 33.3 | 8.3 | 9.4 | 18.2 | 16.1 |
| රෂ් | 2.3 | 0.7 | 0 | 1.9 | 2.5 | 0 | 4.2 | 1.6 | 1.5 | 2.1 |
| වමනය | 2.2 | 2.1 | 25.0 | 1.4 | 2.0 | 0 | 2.1 | 0 | 0 | 1.7 |
| ඕනෑම සෞඛ්ය බලපෑමක් | 39.2 | 19.4 | 0 | 25.2 | 39.1 | 33.3 | 16.7 | 28.1 | 24.2 | 31.8 |
| සාමාන්ය දෛනික කටයුතු කිරීමට නොහැකි වීම | 35.2 | 18.1 | 0 | 22.1 | 33.0 | 33.3 | 10.4 | 25.0 | 15.2 | 28.3 |
| වැඩ කිරීමට හෝ පාසලට යාමට නොහැකිය | 13.7 | 4.9 | 0 | 9.0 | 21.3 | 16.7 | 10.4 | 6.3 | 13.6 | 11.3 |
| අවශ්ය වෛද්ය ප්රතිකාර | 2.1 | 1.4 | 0 | 1.5 | 3.0 | 0 | 6.3 | 0 | 0 | 1.8 |
| ටෙලීඡ්ලියල් | 0.9 | 0.7 | 0 | 0.7 | 1.0 | 0 | 2.1 | 0 | 0 | 0.8 |
| සායනය | 0.7 | 0.7 | 0 | 0.6 | 0.5 | 0 | 4.2 | 0 | 0 | 0.6 |
| හදිසි සංචාරය | 0.2 | 0 | 0 | 0.2 | 0 | 0 | 4.2 | 0 | 0 | 0.2 |
| රෝහල්ගතවීම | 0.05 | 0 | 0 | 0.1 | 0 | 0 | 0 | 0 | 0 | 0.1 |
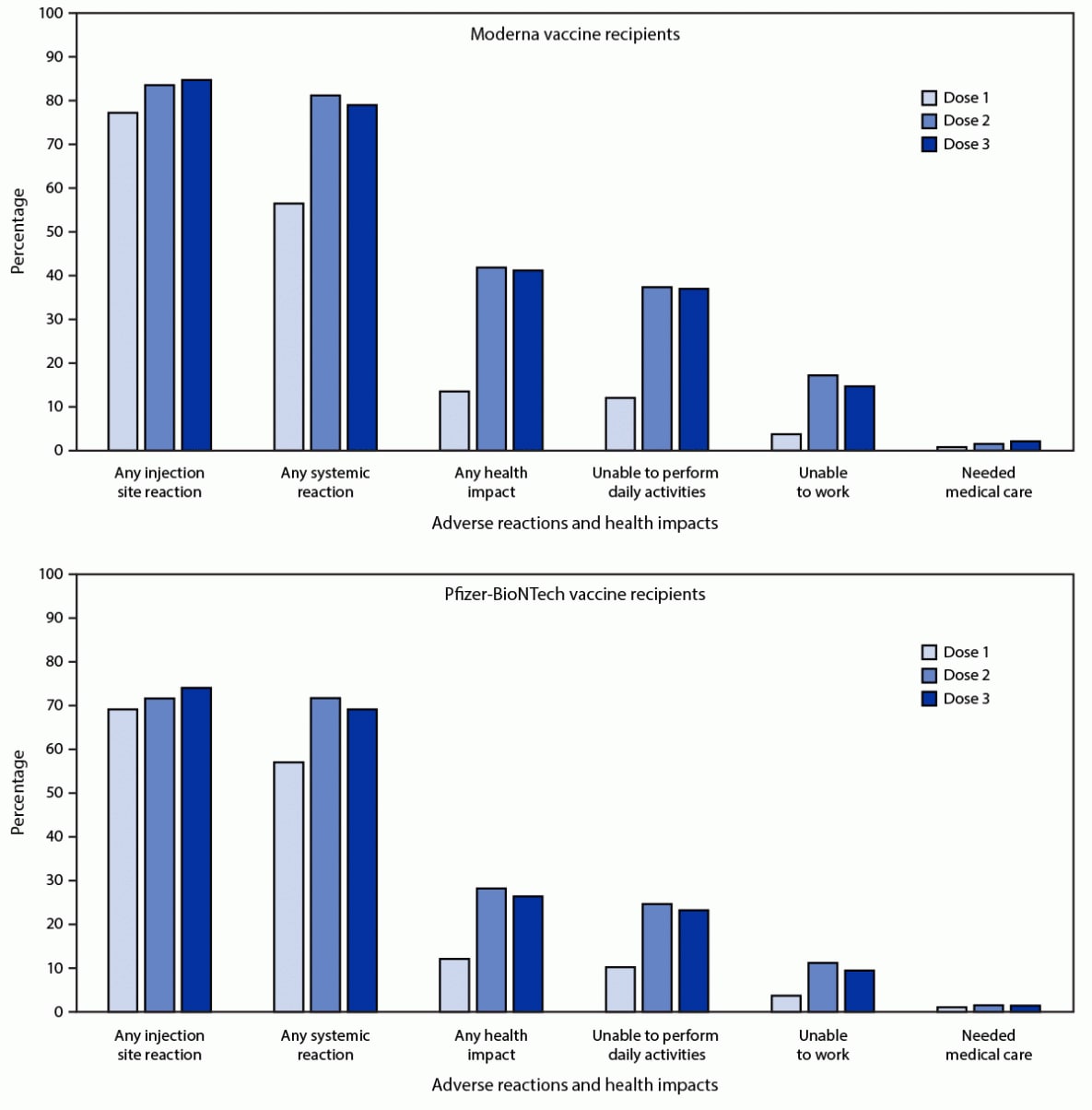
ෆිගර්. මෝඩර්නා (එන් = 3) මාත්රා 6,283 ක් හෝ ෆයිසර්-බයෝඑන්ටෙක් (එන් = 6,308) කෝවිඩ් -19 එන්නත ලබා ගත් අය විසින් වාර්තා කරන ලද අහිතකර ප්රතික්රියා සහ සෞඛ්ය බලපෑම් සහ 0- දින වල අවම වශයෙන් v- ආරක්ෂිත සෞඛ්ය පරීක්ෂණ සමීක්ෂණයක් වත් සම්පූර්ණ කරන්න. එක් එක් මාත්රාවෙන් පසුව, මාත්රා අංකය අනුව - එක්සත් ජනපදය, අගෝස්තු 7 සිට 12 සැප්තැම්බර් 19, 2021 දක්වා
මෙම ලිපියෙන් ඉවත් කළ යුතු දේ:
- Results from a phase 3 clinical trial conducted by Pfizer-BioNTech that included 306 persons aged 18–55 years showed that adverse reactions after receipt of a third dose administered 5–8 months after completion of a 2-dose primary mRNA vaccination series were similar to those reported after receipt of dose 2.
- Persons who reported receiving a primary series from different manufacturers or a manufacturer that was unknown or unavailable in the United States, or 2 doses of vaccine after receipt of a Janssen (Johnson &.
- On August 12, 2021, the Food and Drug Administration (FDA) amended Emergency Use Authorizations (EUAs) for the Pfizer-BioNTech and Moderna COVID-19 vaccines to authorize administration of an additional dose after completion of a primary vaccination series to eligible persons with moderate to severe immunocompromising conditions (1,2).























